Infezione da clamidia nell’uomo e nella donna
SALERNO
L’infezione da clamidia può a volte non presentare sintomi
L’infezione da clamidia rappresenta la causa di uretrite più frequente nell’uomo e nella donna. Essa può decorrere in maniera asintomatica, in quanto vi possono essere portatori asintomatici. Il periodo di incubazione delle infezioni da clamidia può variare da 1 a 2 settimane.
Infezione da clamidia nell’uomo
L’infezione da clamidia nell’uomo, può decorrere senza sintomi o presentarsi con uretrite (infiammazione dell’uretra con eventuale bruciore e arrossamento del meato uretrale), secrezione trasparente sierosa, associandosi talora a fenomeni come orchite monolaterale, epididimite e dolore ai testicoli oppure a proctite, caratterizzata da anite, diarrea e dolore al momento della defecazione. L’obliterazione bilaterale post infiammatoria del dotto deferente può in alcuni casi causare sterilità. La congiuntivite da Chlamydia trachomatis dell’adulto, causata dai sierotipi da D a K, può essere trasmessa o autotrasmessa in entrambi i sessi con le secrezioni genitali e può presentarsi con secrezione e lacrimazione.
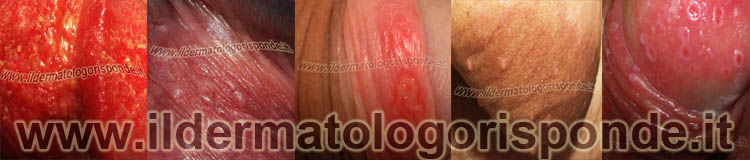
In dermatologia genitale maschile, vanno considerate sia le malattie veneree (foto in alto) che non veneree (foto in basso)
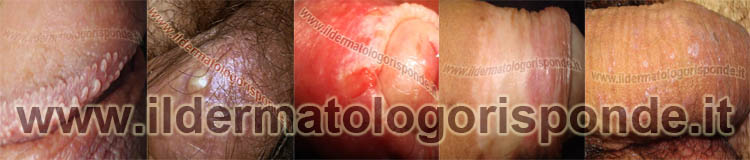
Infezione da clamidia nella donna
L’infezione da clamidia nella donna, può avere un decorso asintomatico o presentarsi con uretrite, leucorrea sierosa, dolore addominale, mestruazioni abbondanti e piccole perdite ematiche non legate al ciclo mestruale. Nella donna, l’infezione da clamidia si può talora associare a endometrite, salpingite, peritonite pelvica e malattia infiammatoria pelvica (PID), fino alla rara complicanza della periepatite venerea, nota come sindrome di Fitz Hugh Curtis. L’infezione da clamidia è la causa più frequente di cervico vaginite e la fibrosi post infiammatoria delle tube di Falloppio può talora causare sterilità o gravidanze extrauterine. Oltre che alle infezioni da clamidia, la malattia infiammatoria pelvica si può talora associare a infezioni da neisseria gonorrhea, gardnerella vaginalis e mycoplasma genitalium. Insieme alla visita venereologica di coppia, è molto importante la visita ginecologica per poter prevenire, ricercare e trattare, possibili complicanze nella donna.
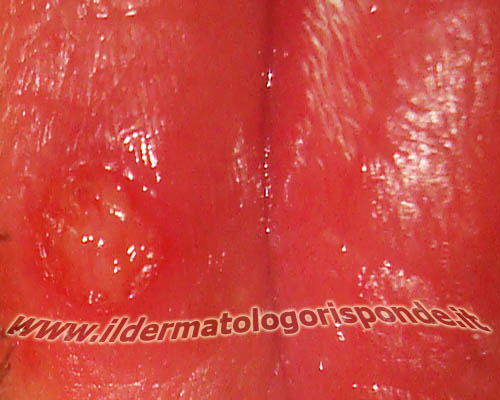
Rispetto all’uretrite da herpes genitale (nella foto), nell’infezione da clamidia, mancano manifestazioni cliniche patognomoniche
Il tampone uretrale nell’uomo e nella donna
La ricerca della clamidia nell’uomo può essere effettuata in laboratorio mediante tampone uretrale effettuato ad alcuni centimetri dal meato uretrale esterno. Alcuni laboratori specializzati, effettuano la ricerca non invasiva della clamidia, mediante PCR (Polymerase Chain Reaction) effettuata sulle urine (mitto urinario iniziale). La ricerca della clamidia nella donna può essere effettuata a livello del collo dell’utero e a livello endouretrale. Anche nella donna, la PCR eseguita sul mitto urinario iniziale è una metodica rapida e non invasiva, rispetto al classico tampone uretrale. Il dosaggio degli anticorpi anticlamidia (es. IgG, IgM, IgA, etc) è poco specifico in caso di semplice uretrite (in quanto l’infezione della sola mucosa uretrale, raramente stimola una risposta anticorpale sistemica), mentre potrebbe essere utile in presenza di infezioni del tratto urogenitale alto, sia nell’uomo (es. orchiepididimite) che nella donna (es. salpingite, peritonite, etc). Tra i vari esami diagnostici per ricerca Clamidia, i test di amplificazione degli acidi nucleici (NAAT = Nucleic Acid Amplification Test), come ad esempio il Chlamydia trachomatis DNA-PCR, possono essere effettuati su un normale campione di urine, su un campione di liquido seminale, o su materiale proveniente da tampone cervico vaginale, tampone uretrale, tampone rettale e tampone faringeo.
Le infezioni da clamidia si possono associare ad altre malattie veneree
Una volta accertata l’infezione da clamidia, il dermatologo al momento della visita specialistica, suggerisce solitamente un checkup completo per escludere una possibile associazione con altre malattie veneree (per esempio papulosi bowenoide, condilomi, herpes genitale, sifilide, ulcera molle, gonorrea, linfogranuloma venereo, granuloma inguinale, HIV, etc). Dopo aver contratto una gonorrea, si può talora osservare un’uretrite post gonococcica da clamidia, dovuta a una doppia infezione (gonococco + clamidia). In questi casi, l’uretrite da clamidia, si presenta dopo alcuni giorni dall’infezione gonococcica, avendo la clamidia un tempo di incubazione più lungo rispetto alla Neisseria gonorrhoeae. Un’infezione da clamidia in gravidanza, può favorire la trasmissione della malattia al neonato in circa il 50% dei casi, con possibile parto prematuro. Nei bambini nati da madri con infezione da clamidia si possono avere diverse complicanze come l’oftalmia neonatale e la polmonite neonatale da Chlamydia trachomatis.
Clamidia e terapia di coppia
Le clamidie sono parassiti intracellulari obbligati gram negativi e sono responsabili di diverse patologie come il tracoma endemico (una delle principali cause di cecità al mondo), il linfogranuloma venereo di Nicolas Favre e le infezioni urogenitali (es. uretrite da clamidia, epididimite da clamidia, salpingite da clamidia, endometrite da clamidia, cervico vaginite da clamidia, proctite da clamidia, etc). I sierotipi A, B, Ba e C infettano prevalentemente la congiuntiva (tracoma endemico). I sierotipi D, Da, E, F, G, Ga, H, I, Ia, J, Ja e K, infettano prevalentemente il tratto urogenitale, mentre i sierotipi L1, L2, L2a, L2b e L3 li riscontriamo nel linfogranuloma venereo. Chlamydia trachomatis esiste in due forme, note come corpi elementari (forma extracellulare ad alta capacità infettiva) e corpi reticolari (forma intracellulare con funzioni replicative). La clamidia possiede sulla sua membrana esterna, speciali proteine in grado di legarsi alle cellule bersaglio. Tra i sistemi di adesione più importanti per la clamidia, ricordiamo le MOMP (major outer membrane proteins), le POMP (polymorhic outer membrane proteins), le proteasi clamidiche (CPAF = chlamydial proteases o proteosome like activity factors), il sistema di secrezione di tipo 3 (TTSS = type three secretion system) e le heat shock proteins (HSP). In particolare le heat shock proteins HSP60 e HSP70 dei corpi elementari, sarebbero responsabili di importanti reazioni di ipersensibilità ritardata, talora possibili cause di aborto spontaneo, nelle donne con infezioni da clamidia in gravidanza. La clamidia, aderisce alle cellule epiteliali umane (es. distretto anogenitale, congiuntiva, etc) con particolare tropismo per l’epitelio cilindrico della cervice uterina, mentre la mucosa della vagina pur non essendo facilmente suscettibile a un legame diretto con il microrganismo, può scatenare una vaginite come risposta infiammatoria alla clamidia. Al momento del rapporto sessuale, il passaggio di liquido seminale, può diffondere nella donna la clamidia dai genitali esterni al tratto urogenitale alto. Le uretriti da clamidia vengono anche indicate come uretriti non gonococciche, insieme alle uretriti da Trichomonas vaginalis, all’uretrite da micoplasma (es. Ureaplasma urealyticum), all’uretrite da candida e da herpes genitalis. I sierotipi D, E ed F, causano oltre i 2/3 delle infezioni urogenitali da clamidia. L’infezione da clamidia è una malattia della coppia ed è importante esaminare anche il partner o la partner, per programmare eventuale prevenzione o terapia di coppia.
Le infezioni da clamidia attraverso la storia
Già nel 60 d.C il medico siciliano Dioscoride Pedanio, utilizza il termine tracoma (dal greco trākhus = ruvido) per descrivere un’infezione dell’occhio da Chlamydia trachomatis, caratterizzata da rossore, granulazione, bruciore, lacrimazione, fotosensibilità e in alcuni pazienti, persino cecità. Nel 1879, il medico svizzero Jacob Ritter descrive la psittacosi (nota anche come ornitosi), altra malattia infettiva causata da clamidia (Chlamydophila psittaci) e trasmessa dagli uccelli all’uomo, chiarendone i tempi di incubazione della malattia ed escludendone una possibile trasmissione venerea. Nel 1907 il radiologo tedesco Ludwig Halberstädter e il batteriologo austriaco Stanislaus Josef Mathias Edler von Prowazek, durante uno studio condotto a Giava, inoculano nella congiuntiva degli orangutan, materiale proveniente dai pazienti affetti da tracoma. Prowazek pensa inizialmente a un nuovo tipo di microrganismo simile ai protozoi che chiama chlamydozoaria (dal greco χλαμύς = mantello) per descrivere la caratteristica disposizione delle clamidie a ridosso del nucleo, di colore rosso alla colorazione Giemsa e ricoperte da un mantello di colore blu. Nel 1911 l’oftalmologo austriaco Karl Lindner, osserva le stesse inclusioni cellulari del tracoma endemico, nelle infezioni urogenitali. Nel 1930 il virologo americano Ralph Dougall Lillie, descrive accuratamente la psittacosi. Negli stessi anni, il colonnello medico americano Thomas Fitz Hugh e il ginecologo americano Arthur Hale Curtis descrivono una rara complicanza della malattia infiammatoria pelvica, caratterizzata da peritonite e periepatite (periepatite venerea), in seguito denominata sindrome di Fitz Hugh Curtis, confermando gli importanti studi iniziati nel 1920 dal chirurgo uruguaiano Carlos Stajano. Nel 1932 viene chiarito lo sviluppo bifasico della clamidia in corpi elementari e corpi reticolari, con un importante studio del batteriologo britannico Sir Samuel Phillips Bedson, che è anche il primo ricercatore a ipotizzare l’appartenenza dell’agente eziologico ai batteri, concetto che sarà poi confermato circa 30 anni più tardi. Nel 1934, l’oftalmologo americano Phillips Thygeson, studia le analogie istologiche tra la congiuntivite da tracoma endemico e la psittacosi. Nel 1935, l’oftalmologo italiano Archimede Busacca, descrive la clamidia utilizzando il termine chlamydozoon trachomatis. Studi molto importanti sulle clamidie sono stati effettuati da Machiacello nel 1944 e dal microbiologo canadese Geoffrey Rake nel 1957. Il tracoma virus (la natura batterica della clamidia sarà chiarita negli anni successivi) viene isolato nel 1957 in Cina dal gruppo di studio di T’ang, in un esperimento condotto sul sacco embrionale di pulcino. L’anno successivo il virus viene inoculato in volontari umani per confermarne il ruolo eziologico nella congiuntivite da tracoma e nelle infezioni genitali. In quanto agenti filtrabili, si riteneva in passato che le clamidie fossero dei grossi virus atipici e non dei batteri, fino a quando nel 1964 Stanier e Moulder osservano mediante microscopio elettronico, che esse contengono oltre al DNA e all’RNA, strutture come ribosomi e parete cellulare. Nel 1965 viene isolato dalla congiuntiva di in un bambino del Taiwan un sierotipo di clamidia denominato TWAR (TaiWan Acute Respiratory) come causa di infezioni respiratorie. Nel 1966 Page, separa il genere Chlamydia dalle Rickettsie, fino ad allora raggruppati insieme. Importanti studi sulle infezioni genitali da clamidia furono condotti nel 1964 da Jones, nel 1971 da Darouger e nel 1974 da Hilton. Nel 1986, Chlamydia pneumoniae viene riconosciuto come patogeno delle vie respiratorie. Nel 1998 viene sequenziato l’intero genoma del sierotipo D della clamidia, dal gruppo di lavoro di Richard Scott Stephens. Dal 1999 la famiglia delle Chlamydiaceae è suddivisa in 2 generi, noti rispettivamente con il nome di Chlamydia e like Chlamydia (o Chlamydophila secondo Hans Truper e Johannes Storz).
